捕捉人类的古老起源 古DNA检测
古DNA检测

DNA 是我们世界中看不见的常数。不仅它的 As、Ts、Cs 和 G 构成了地球上所有生命的基础,而且从生物身上脱落的 DNA 将渗透到我们周围的环境中,在某些情况下,它们会比我们活得更久。
作为一种生物材料,DNA 非常稳定。当储存在凉爽干燥的气候中时(例如洞穴深处,坐落在矿化骨骼中),DNA 可以稳定数十万年1.因此,在出土的古代人类遗骸中可以找到 DNA 也就不足为奇了,这为研究人员提供了一扇了解过去的窗口,研究人员可以通过它来研究我们的进化历史。
古代 DNA 的前景在于其信息承载能力。存储在 DNA 中的模式可以告诉我们古代原始人的生活、他们那个时代的人口动态,以及现代人类是如何形成的。但是,从这些风化样本中提取这些信息并非易事。这不仅在技术上具有挑战性,而且提取 DNA 的过程是破坏性的,这意味着这些珍贵的文物即使不是彻底销毁,也必须被破坏。因此,在处理古代 DNA 时,对错误的容忍度很小——即使是很小的低效率也会造成无法弥补的损失。由于风险如此之高,研究人员能够获得最适合这项工作的工具至关重要。
用于窥视过去的工具
1984 年,加州大学伯克利分校的研究人员使用分子克隆技术产生了世界上第一个古老的 DNA 序列:<从保存下来的 140 年历史的鲑鱼标本 (Equus quagga)2.在对马的进化历史进行有趣的揭示的同时,这项研究被证明是基础概念证明,即即使是过时的 DNA 也可以提供有关过去的宝贵信息,从而建立古基因组学的新领域。
分子克隆可能使我们首次涉足古基因组学,但随着更先进的测序技术的采用,它很快就被搁置了3,4.现在,就像外科医生伸手去拿手术刀一样,研究古代 DNA 的研究人员通常会在新一代测序 (NGS) 上游寻找靶向富集检测组合,以帮助他们从古代样本中提取可靠的数据。
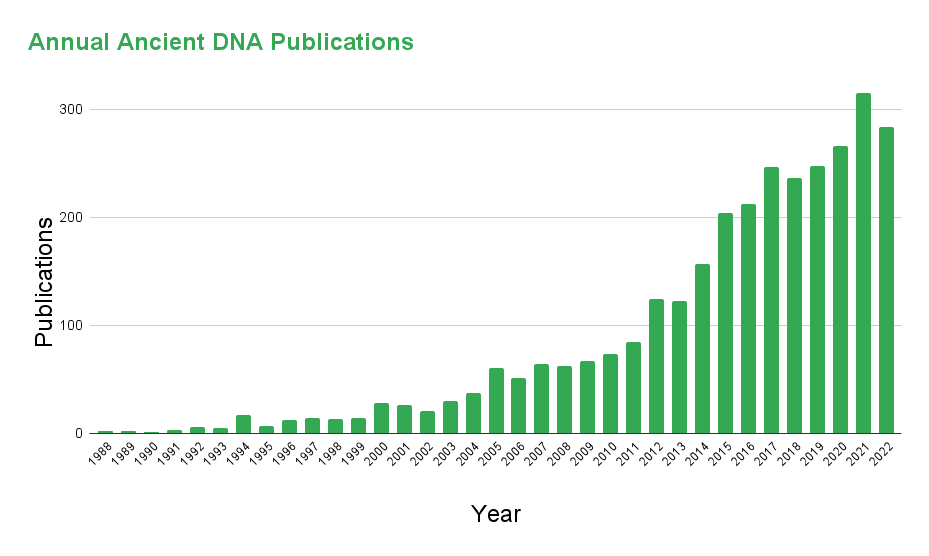
与早期技术(如分子克隆和 PCR)的局限性相比,NGS 可实现大规模平行测序和广泛的覆盖面,因此可以在一次运行中对个体的整个基因组进行测序。NGS 技术于 2006 年首次用于古代 DNA 分析,对从 28,000 年前的长毛猛犸象中提取的 ~13 Mb DNA 和从尼安德特人中提取的 ~1Mb DNA 进行了测序4.NGS 提供的测序信息的巨大收益催化了古基因组学的繁荣(见图 1))。
然而,尽管 NGS 具有所有优势,但 NGS 可能是一个极其昂贵的过程,尤其是在古基因组学研究方面。通常,古代 DNA 占出土遗骸中发现的 DNA 总量的不到 10%,其余 90%(通常更多)由细菌、真菌或现代人脱落的外源 DNA 组成4.如果 NGS 技术的应用不带偏见,将花费大量资源对这种信息量不足、污染严重的 DNA 进行测序。这就是靶向富集 NGS(以下简称靶向 NGS)的益处所在。
古基因组学中的靶向 NGS panel
靶向 NGS 使研究人员能够将测序资源集中在他们研究感兴趣的遗传片段上。这通常是通过合成生物素化寡核苷酸探针来完成的,这些探针被设计为与特定靶序列互补。当与样品 DNA 一起孵育时,这些寡核苷酸探针将与它们的互补靶序列结合。然后添加链霉亲和素包被的磁珠可以固定探针及其结合的任何序列。样品中剩余的 DNA 可以被洗掉,只留下目标的结合片段。
通过去除多余的 DNA,研究人员能够将测序资源集中在特定的基因组靶标上,从而获得更深的测序覆盖度。这通常意味着以更少的资本投资获得更准确的测序结果(请参阅我们最近的博客,了解靶向富集的好处以了解更多信息)。
要了解靶标富集在研究 aDNA 中的巨大潜力,请考虑一些粗略的数学运算。要以标准的 30 倍覆盖度对现代人类基因组进行全基因组测序,需要大约 4 亿个测序读长。然而,古代 DNA 样本经常被无数非人类 DNA 污染。而且,存在的古人类 DNA 经常被降解,因此只有不到 1% 的序列产生可用数据。为了使用广泛的非靶向策略实现对目标变体的必要覆盖,需要将总测序读数推高到数十亿个,这很快就会使实验成本高昂且不切实际。通过富集,我们可以仅靶向感兴趣的变异区域,同时去除大部分污染的 DNA 序列。因此,研究人员可以从古代样本中的数十万个变体中提取有价值的信息,每个样本只需 2500 万个读数。
自 2015 年以来,古基因组学领域在很大程度上依赖于一种称为“1240k 试剂”的特定靶向富集面板,该试剂是一组寡核苷酸探针,旨在捕获包含 124 万个被认为具有信息量的多态性中的任何一个的 DNA 片段。截至 2022 年 10 月,该面板已用于生成全球全基因组古人类 DNA 数据>70%5.
尽管 1240k 试剂是一种广泛使用的工具,但存在局限性,包括富集有效性的可变性、等位基因捕获的偏差,以及由于没有商业产品,合成靶探针集的成本很高5.总的来说,这些限制都使得难以比较该领域的数据集,并阻止了除少数实验室外的所有实验室都参与古 DNA 的全基因组研究。为了减少这些问题,领先的研究人员致力于改进古代 DNA 靶向富集检测组合的设计和可及性。
🧬 DNA 衰变的类型
DNA 随着时间的推移而降解的方式有很多种。以下是其中的几个:
- 片段化:糖磷酸骨架和嘌呤碱基之间的化学键易水解,导致 DNA 链中出现脱碱基位点。反过来,非碱基位点会导致链断裂。这就是为什么古代 DNA 在提取时通常会产生短片段的原因。
- 脱氨作用:DNA 衰变的另一种自然形式是胞嘧啶脱氨为尿嘧啶碱基。这是一个重要的变化,因为它将导致聚合酶在复制过程中掺入碱基取代,从而导致 C 到 T 和 G 到 A 的取代。这两者都可能混淆序列分析。
- 病变:DNA 可能会发生许多不同的修饰,从而导致交联。这种修饰可以阻止酶执行其功能并防止 DNA 链复制。
在本次网络研讨会中了解 Twist 如何帮助研究人员解决 DNA 衰变问题并挖掘我们的古老历史:使用 Twist 技术高效富集 140 万个 SNP 靶标,用于古代 DNA 分析
Twist Ancient DNA 检测组合
2021 年,Twist Bioscience 为 aDNA 制作了一种市售的靶向富集组合,该组合可富集 1240k 试剂涵盖的 124 万个多态性,以及其他感兴趣的内容。哈佛大学的 Nadin Rohland、Swapan Mallick、Matthew Mah、Robert Maier、Nick Patterson 和 David Reich 着手对他们设计的使用 1240k 试剂和另一种市售检测组合设计的优化 Twist 古代 DNA 检测组合进行独立比较5.结果表明,Twist 的检测组合提供了高度均匀的覆盖度,对片段长度的偏差较小,总体 SNP 覆盖度增加了 1.2 到 1.4 倍,并且能够提供如此高质量的数据,以至于它可以与鸟枪法测序数据进行共同分析,而不会产生实质性的偏差(这是该领域长期存在但未满足的需求)。
Twist Ancient DNA 检测组合的高性能使得哈佛大学实验室已经不再使用 1240k 试剂,转而使用更新的优化检测组合,使用 Twist 试剂已经超过 10,000 次5,6.作为一种市售资源,Twist 的 panel 有助于消除合成靶标富集探针的经济负担,并为更广泛地参与古基因组学研究打开了大门。
References
- Allentoft, Morten E., et al. “The Half-Life of DNA in Bone: Measuring Decay Kinetics in 158 Dated Fossils.” Proceedings of the Royal Society B: Biological Sciences, vol. 279, no. 1748, 10 Oct. 2012, pp. 4724–4733, https://doi.org/10.1098/rspb.2012.1745.
- Higuchi, Russell, et al. “DNA Sequences from the Quagga, an Extinct Member of the Horse Family.” Nature, vol. 312, no. 5991, Nov. 1984, pp. 282–284, ui.adsabs.harvard.edu/abs/1984Natur.312..282H, https://doi.org/10.1038/312282a0.
- Danielewski, Mikołaj, et al. “Methodological Changes in the Field of Paleogenetics.” Genes, vol. 14, no. 1, 16 Jan. 2023, p. 234, https://doi.org/10.3390/genes14010234.
- Shapiro, B., and M. Hofreiter. “A Paleogenomic Perspective on Evolution and Gene Function: New Insights from Ancient DNA.” Science, vol. 343, no. 6169, 23 Jan. 2014, pp. 1236573–1236573, science.sciencemag.org/content/343/6169/1236573.full, https://doi.org/10.1126/science.1236573.
- Rohland, Nadin, et al. “Three Assays for In-Solution Enrichment of Ancient Human DNA at More than a Million SNPs.” Genome Research, vol. 32, no. 11-12, 1 Nov. 2022, pp. 2068–2078, https://doi.org/10.1101/gr.276728.122.
- Liu, Yue-Chen, et al. “Ancient DNA Reveals Five Streams of Migration into Micronesia and Matrilocality in Early Pacific Seafarers.” Science, vol. 377, no. 6601, July 2022, pp. 72–79, https://doi.org/10.1126/science.abm6536.
原英文链接
Capturing the ancient origins of humanity | Twist Bioscience
推荐文章
-
Twist推出的多基因片段库(Multiplexed Gene Fragments)首次突破300 bp的传统合成极限,实现500 bp长片段的高通量合成。
-
低起始量样本的靶向甲基化测序通常存在相当大的挑战,因为未甲基化胞嘧啶的转化降低了基因组测序的复杂度。Twist 的甲基化检测系统通过组合探针的能力(可以实现不同级别的优化过滤严谨度)有效地克服了这些障碍,同时还引入了甲基化促进剂,这是一种定制的阻断剂,通过减少脱靶来产生协同作用,以提高系统性能。这两种优化都极大地提高了甲基化检测组合观测到的测序性能,促进了 Twist 甲基化检测系统可支持液体活检等高灵敏度应用的改进。...
-
专家视角|Julian Jude谈功能基因组学的新时代 市场部 Twist Bioscience 拓唯思特 2025年02月18日 17:30 北京 当下正是功能基因组学研究的黄金时代。CRISPR技术工具库的持续扩展,使研究者能以更复杂、更大规模的方式操控基因组;人工智能(AI)助力多模态数据分析,不仅能优化功能筛选设计,还能从中挖掘更深层的生物学意义。如今,功能基因组学研究已迈入规模化与高效化并行的新纪元。这些划时代的进步,离不开合成DNA制备技术的同步革新——这一常被忽视的技术,实为现代分子生物学的基石。 近期,我们与Julian Jude博士 深入探讨了过去十年合成DNA技术的演进,以及它如何推动当今功能基因组学的蓬勃发展。 专家简介 Julian是功能基因组学领域的资深专家,拥有20余篇学术论文及多项专利申请。在攻读博士及博士后期间,他开发了用于靶点识别的新型功能基因组学工具,主导了70余项全基因组shRNA与CRISPR筛选项目,并参与创建了CRISPR单导RNA(sgRNA)设计评分...